O ministro do STF (Supremo Tribunal Federal) Ricardo Lewandowski deu prazo de 48 horas para que a Anvisa (Agência Nacional de Vigilância Sanitária) dê informações sobre os critérios usados para os testes da vacina Coronavac e o atual estágio de aprovação desta e demais vacinas contra a Covid-19.
Em despacho publicado nesta terça-feira (10), o ministro determina que a agência preste informações complementares.
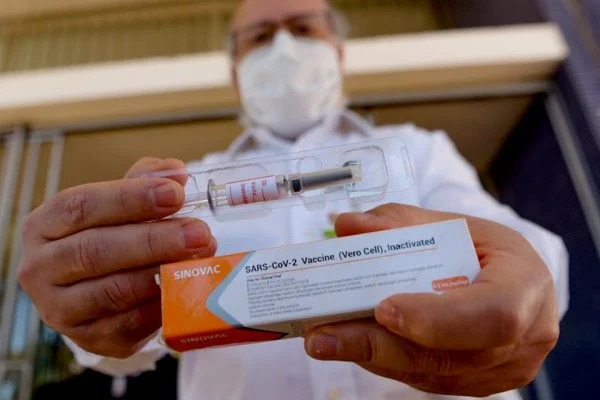 Segundo o diretor-presidente da Anvisa, Antônio Barra Torres, a medida foi tomada por causa de uma “decisão técnica” – Foto: Jacqueline Lisboa/MetropolesS
Segundo o diretor-presidente da Anvisa, Antônio Barra Torres, a medida foi tomada por causa de uma “decisão técnica” – Foto: Jacqueline Lisboa/MetropolesS“Determino que a Anvisa, observado o âmbito de sua autonomia técnica, preste informações complementares àquelas já ofertadas pela Presidência da República e pela Advocacia-Geral da União, acerca dos critérios utilizados para proceder aos estudos e experimentos concernentes à vacina acima referida, bem como sobre o estágio de aprovação desta e demais vacinas contra a Covid-19”, afirmou Lewandowski, no despacho.
SeguirA agência determinou na segunda-feira (9) a interrupção dos estudos da vacina Coronavac por causa de “evento adverso grave”.
A vacina é produzida pelo Instituto Butantan e pela farmacêutica chinesa Sinovac. Segundo comunicado, o evento – não especificado – aconteceu em 29 de outubro.
A decisão da suspensão da pesquisa acontece para que os estudos possam avaliar sobre a segurança e benefícios à saúde do possível imunizante antes da continuidade do estudo.
Nesta terça (10), o governo de São Paulo afirmou que a morte de voluntário que participava de estudo não tinha a ver com os testes.
Segundo o diretor-presidente da Anvisa, Antônio Barra Torres, a medida foi tomada por causa de uma “decisão técnica” diante de “informações insuficientes” sobre um evento adverso grave ocorrido com um dos participantes da pesquisa.
Torres afirmou que é normal a paralisação dos estudos em testes de vacina. Ele citou o caso do imunizante de Oxford, que também interrompeu sua pesquisa por causa de um evento adverso.


