A Comissão Temporária da Covid-19 do Senado debateu nesta sexta-feira (7) sobre a aquisição da vacina russa Sputnik V. No dia 26 de abril, a Anvisa negou a autorização para a importação e uso emergencial do imunizante.
O representante da farmacêutica União Química, Fernando Marques, responsável pela vacina da Sputnik V no Brasil, e por enviar os dados de eficácia e segurança para a Anvisa (Agência Nacional de Vigilância Sanitária), disse que a empresa vai apresentar um novo pedido para uso emergencial de mais 10 milhões de doses da vacina no país.
Ele também declarou que “já que não perdemos esses 10 milhões (de doses) que não pudemos importar no primeiro trimestre, conseguimos 10 milhões com o governo russo embarcando de lá. Ao mesmo tempo, o nosso processo industrial está caminhando”.
Seguir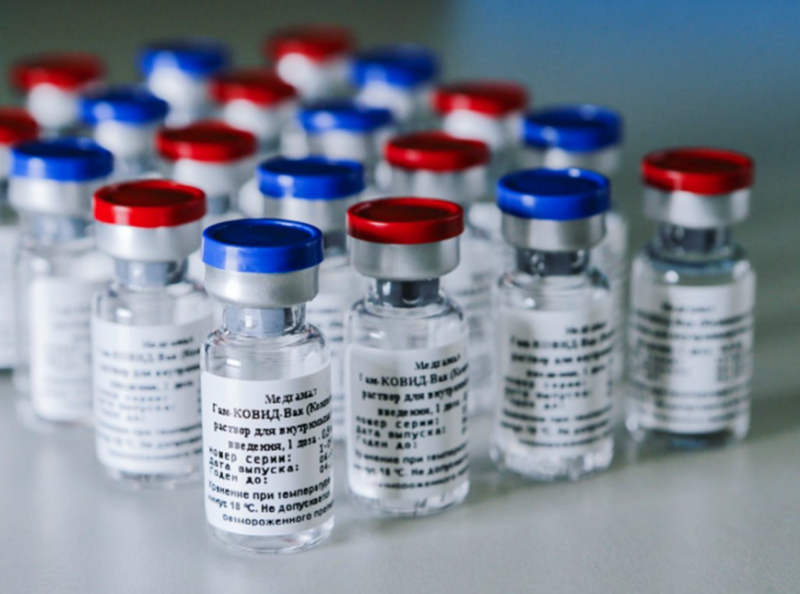 Governadores pedem nova análise da vacina russa Sputnik V – Foto: Divulgação/Sputnik V
Governadores pedem nova análise da vacina russa Sputnik V – Foto: Divulgação/Sputnik VA diretora da Anvisa, Meiruze Freitas, declarou que o órgão está sempre aberto ao diálogo. “Ainda há processos em discussão, inclusive, com os importadores”, disse em audiência pública da Comissão Temporária da Covid-19 do Senado, que debateu a aquisição de vacinas pelo Brasil.
Durante a audiência, o representante do Consórcio Nordeste e governador do Piauí, Wellington Dias, atribuiu o não cumprimento do plano de vacinação, feito pelos Estados em 2020, a não aprovação do imunizante pela agência. O plano previa que, em 30 de abril deste ano, pelo menos 25% da população brasileira estaria vacinada.
O relator da matéria sobre a importação da Sputnik V na Anvisa, Alex Campos, disse aos senadores que a agência trabalha com modalidade regulatória excepcional para vacinas com um rito mais acelerado.
Campos também destacou que não foi apresentado relatório técnico da vacina à Anvisa, que notificou todos os importadores, enviando expediente para 62 países que aprovaram o uso emergencial da Sputnik para saber os motivos das aprovações. A garantia da eficácia, segurança e qualidade, indispensáveis ao processo, também não foi apresentada à agência.