O Ministério da Saúde recebeu um requerimento assinado por 45 médicos contestando nota técnica da Anvisa sobre a situação das vacinas contra Covid-19 perante a autoridade regulatória, no que diz respeito ao status de segurança e eficácia.
Seguem trechos do documento:“(…) Na Nota Técnica n.º 496/2021/SEI/GGMED/DIRE2/ANVISA, de 23 de dezembro de 2021, a Anvisa afirma que ‘as vacinas contra Covid-19 autorizadas no Brasil não são experimentais, tendo todas cumprido com as etapas de desenvolvimento clínico completo’.
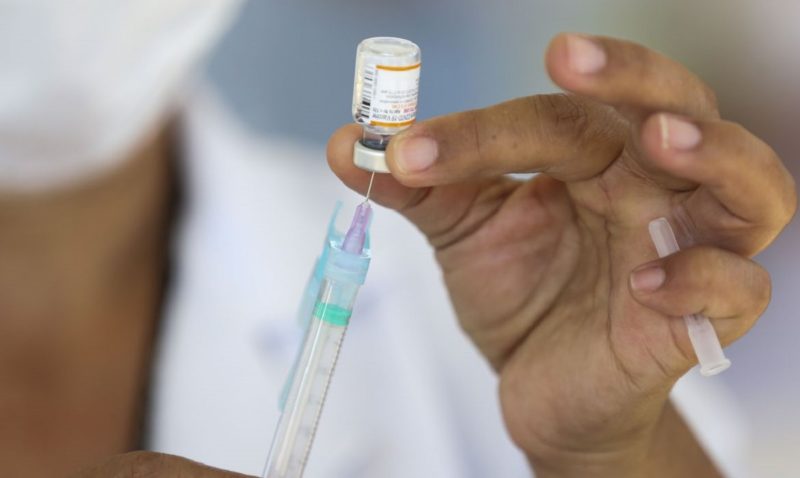 Vacinação contra a Covid-19 – Foto: José Cruz/Agência Brasil/ND
Vacinação contra a Covid-19 – Foto: José Cruz/Agência Brasil/NDEssa afirmação não é verdadeira e a Anvisa, ao insistir nessa teoria, contraria os seus próprios regulamentos (…) quando afirma que, ‘para o uso emergencial e para o registro de qualquer vacina, são exigidos dados de estudos de fases III, confirmatórios de eficácia e segurança’.”
Seguir“Ao conceder o registro ‘definitivo’ para a vacina COMIRNATY/PFIZER em 23 de fevereiro de 2021, a Anvisa sabia que os estudos ainda eram precários e que não havia confirmação de eficácia nem de segurança. A agência reguladora norte-americana Food and Drug Administration (FDA), na mesma data, considerava o produto EXPERIMENTAL.
Ora, se não existem os dados conclusivos de fase III dos estudos C4591001 e BNT162-01, a Anvisa não poderia afirmar que o fármaco analisado nos estudos não é Experimental.”
O requerimento ao Ministério da Saúde concentra seus questionamentos na vacina do fabricante Pfizer por ser a única aprovada para crianças e adolescentes no Brasil.
Prossegue o documento:“(…) O parecer público de aprovação do produto COMIRNATY/PFIZER estabeleceu diversos pontos de segurança e eficácia que não restaram comprovados pela fabricante, conforme: a) eficácia e segurança em população pediátrica, gestantes e indivíduos imunossuprimidos; b) administração concomitante com outras vacinas; c) eficácia contra infecção assintomática e transmissão do vírus SarsCov-2;d) eficácia contra Covid-19 grave; e) eficácia contra infecção por variantes de interesse do vírus SarsCov-2; ef) eficácia e segurança em longo prazo.”
O requerimento destaca o termo de compromisso pelo qual a fabricante deverá comprovar a eficácia e segurança do produto até 31 de janeiro de 2024: “Como pode a Anvisa afirmar que o produto não é experimental e que a segurança e eficácia já estão comprovadas, se o registro sanitário ‘definitivo’ foi concedido sob a condição de que a empresa teria até janeiro de 2024 para concluir os estudos e provar a segurança e eficácia da COMIRNATY/PFIZER?”
Entre os 45 médicos que assinam o requerimento estão a Dra. Maria Emília Gadelha Serra (especialista em perícias médicas), o Dr. Edmílson Migowski (infectologista), o Dr. João Jackson Duarte (cardiologista) e o Dr. José Augusto Nasser (neurocirurgião).


